Bacilli Alcol-Acido Resistenti (BAAR) - AFB (Acid-Fast Bacillus)
Noto anche come: AFB (Acid-Fast Bacillus) Coltura, Esame colturale per la tubercolosi, Esame microscopico per la tubercolosi, Mycobacteria tuberculosis Nucleic Acid Amplification Test (TB NAAT), Ricerca dei bacilli alcool-acido resistenti (BAAR), Test molecolari per l’identificazione di Mycobacterium tuberculosis, Test di sensibilità ai farmaci antitubercolari
Nome ufficiale: Ricerca ed identificazione dei bacilli alcool-acido resistenti (BAAR); Test di sensibilità ai farmaci antitubercolari
Ultima Revisione: 11.03.2019
Ultima Modifica: 11.03.2019
Articolo approvato dal Comitato editoriale di labtestsonline.org ed in corso di revisione da parte del Comitato editoriale italiano
In Sintesi
Perché?
Come supporto alla diagnosi e all’identificazione di infezioni causate da Mycobacterium tuberculosis, agente eziologico della tubercolosi (TB o TBC), e di altri bacilli appartenenti alla specie Mycobacterium, noti con il nome di bacilli alcol-acido resistenti (BAAR) o acid-fast bacilli (AFB); per il monitoraggio dell’efficacia del trattamento terapeutico.
Quando?
Nel caso in cui siano presenti segni e sintomi di infezioni polmonari, come tosse cronica, perdita di peso, febbre, brividi e senso di stanchezza, che potrebbero essere riconducibili a infezioni da micobatteri tubercolari o non tubercolari. Il test viene effettuato anche in seguito a positività per i test di screening per la TBC (Test IGRAo test cutaneo della tubercolina) nel caso in cui il paziente sia ad alto rischio di progressione verso la malattia conclamata; nel caso in cui siano presenti sulla pelle o in altre sedi delle infezioni che potrebbero essere dovute al micobatterio; in corso di terapia per TBC.
Il campione
Nel caso in cui si sospetti la TBC polmonare, viene richiesto un campione di escreato generalmente raccolto la mattina presto in giorni differenti. Nel caso in cui la persona affetta non sia in grado di raccogliere autonomamente il campione, può essere raccolto un campione di fluido durante una procedura chiamata broncoscopia (broncoaspirato). Nei bambini può essere raccolto un campione di aspirato/lavaggio gastrico. Se i sintomi sono indicativi per la presenza dell’infezione in altre sedi dell’organismo, possono essere necessari campioni di urina, liquido cefalorachidiano, tessuti bioptici o raccolta di altri fluidi corporei o aspirati provenienti dalla sede dell’infezione.
La preparazione
No, nessuna.
L'Esame
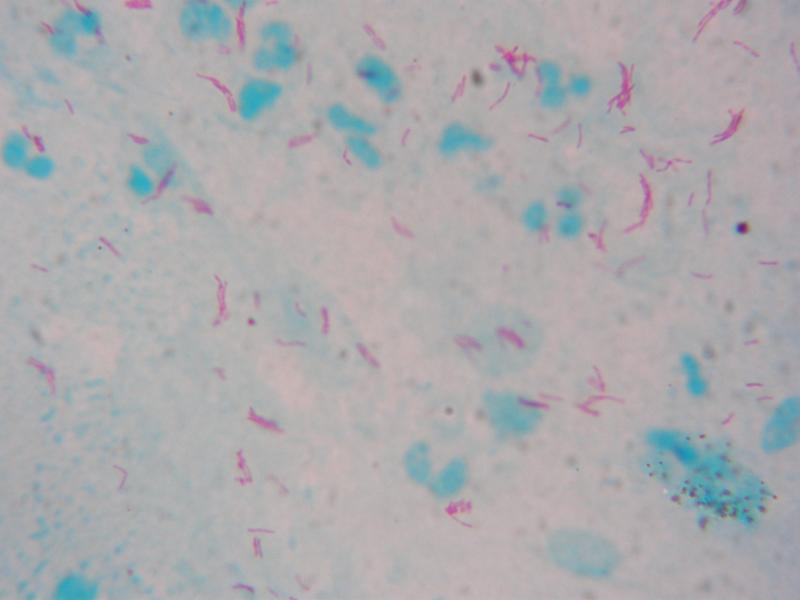
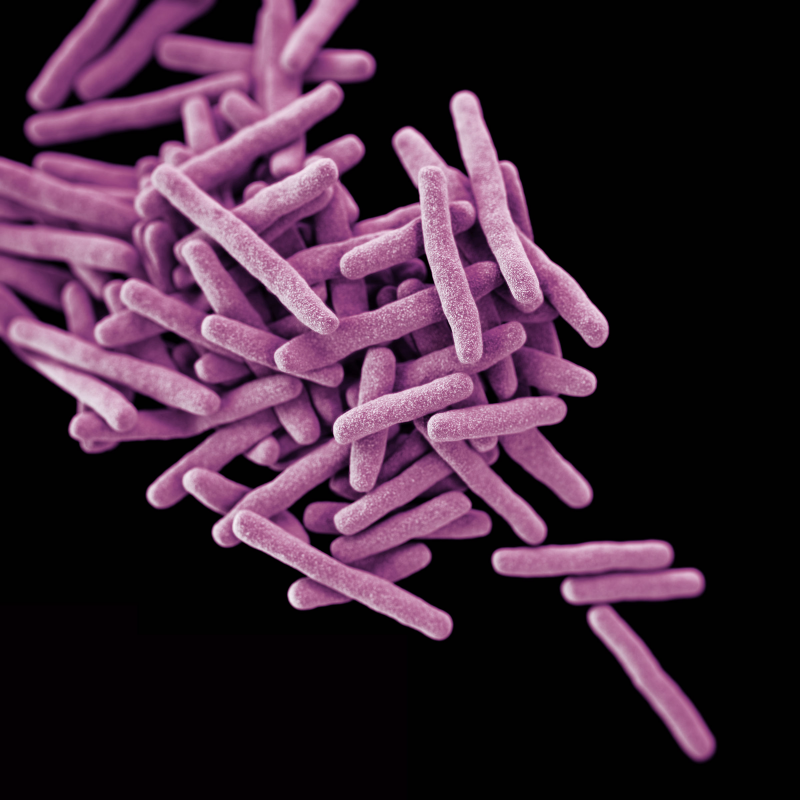
La maggior parte dei campioni che vengono utilizzati per la ricerca ed identificazione dei bacilli alcool- acido resistenti (BAAR) provengono da pazienti con sospetta tubercolosi (TBC) polmonare causata da Mycobacterium tuberculosis. I micobatteri sono noti con il nome di bacilli (batteri a forma di bastoncello) alcol-acido resistenti (BAAR) per la loro capacità di trattenere il colorante utilizzato per l’analisi microscopica in seguito ad un lavaggio effettuato con una soluzione acida. I test per la ricerca ed identificazione dei BAAR sono pertanto un utile supporto alla diagnosi di un’infezione sostenuta dai micobatteri.
Esistono molti tipi di BAAR rilevabili tramite questi esami; tuttavia quelli di maggiore interesse clinico sono i batteri appartenenti al genere Mycobacterium. Il Mycobacterium tuberculosis è il micobatterio maggiormente responsabile della TBC nel nostro paese.
Viste le sue modalità di trasmissione, la TBC viene considerata una malattia a rischio per la salute pubblica. Essa infatti può essere trasmessa da persona a persona per via aerea, tramite gli starnuti, i colpi di tosse ecc…. Può anche creare dei focolai epidemici localizzati, come nelle scuole, negli asili o nelle carceri. Sono particolarmente a rischio di contagio i bambini, gli anziani o le persone con malattie croniche in grado di compromettere la normale funzionalità del sistema immunitario, come l’AIDS. I test di ricerca dei BAAR permettono di limitare la diffusione della TBC e di valutare l’efficacia dei trattamenti terapeutici.
Esiste un altro gruppo di micobatteri noti con il nome di micobatteri non tubercolari. Sebbene a questo gruppo appartengano più di 60 specie di micobatteri, solo un numero ridotto è in grado di infettare l’uomo. Alcuni esempi includono il Mycobacterium avium-intracellulare complex (MAC) responsabile di
infezioni polmonari in persone con il sistema immunitario compromesso, e il Mycobacterium marinum, che può causare infezioni della pelle. I test per la ricerca ed identificazione dei BAAR possono essere utilizzati anche per la diagnosi delle infezioni operate dai micobatteri non tubercolari.
Come e Perchè
Il M. tuberculosise il M. avium infettano generalmente i polmoni, pertanto l’escreato è il campione testato con maggiore frequenza. L’escreato è il muco denso che viene espettorato dai polmoni. Di solito, per aumentare le possibilità di rilevare il micobatterio, vengono raccolti tre campioni in tre mattine consecutive.
Nel caso in cui il paziente non sia in grado di produrre spontaneamente l’escreato, il clinico può raccogliere il campione tramite una procedura chiamata broncoscopia. La broncoscopia permette al clinico di guardare bronchi e bronchioli e di effettuare la raccolta di campioni in queste sedi. Per l’esecuzione della procedura, viene spruzzato nelle vie aeree superiori del paziente un anestetico locale e quindi viene inserita una sonda nei bronchi e nei bronchioli tramite la quale il campione di fluido necessario all’esecuzione del test può essere aspirato. Talvolta può essere prima introdotta, tramite la sonda, una piccola quantità di soluzione salina così da eseguire un lavaggio bronchiale e raccogliere il campione.
Nei bambini piccoli, vista la difficoltà nel produrre l’escreato, viene raccolto un campione di lavaggio/aspirato gastrico. A questo scopo, viene introdotta una piccola quantità di soluzione salina nello stomaco che poi viene aspirata.
Nel caso in cui il clinico sospetti la presenza di TBC extrapolmonare, piuttosto frequente nei pazienti affetti da AIDS, può richiedere l’esecuzione dell’esame sui tessuti o fluidi corporei interessati dall’infezione. Per esempio, in caso di sospetta TBC renale può essere richiesto un campione di urina. Il prelievo di fluidi corporei dalle articolazioni o da altre cavità come l’addome o il pericardio, viene effettuato tramite un ago. Talvolta l’esame può essere eseguito su un campione di liquido cefalorachidiano o su un campione bioptico.
Domande Frequenti
Si, esistono molte persone con un’infezione latente e quindi asintomatiche per TBC. Queste persone sono state esposte al micobatterio ma il loro sistema immunitario l’ha confinato nei polmoni in una forma inattiva. Le persone con un’infezione latente non sono né malate né contagiose, ma il micobatterio è comunque presente e vivo.
Le persone con un’infezione latente risultano positive al test cutaneo della tubercolina e al test IGRA. La maggior parte delle persone con un’infezione latente, circa il 90%, non progredirà mai verso laTBC.
Anche i pazienti affetti da TBC e quindi con un’infezione attiva possono essere asintomatici nelle fasi iniziali della malattia. I primi sintomi possono essere subdoli e, nel caso di TBC extrapolmonare (in organi come i reni o le ossa), la TBC può essere asintomatica anche in stadi piuttosto avanzati della malattia.
Immagini Correlate
Pagine Correlate
In questo sito
Altrove sul web
Ministero della salute - MANUALE TECNICO PER LA DIAGNOSI MICROBIOLOGICA DELLA T…
Scheda Tubercolosi - Ministero della Salute
Tubercolosi - Ministero della Salute
Centers for Disease Control and Prevention: Tuberculosis
CDC: Traveler's Health Yellowbook - Tuberculosis
World Health Organization: Tuberculosis
MedlinePlus Medical Encyclopedia: Mycobacterial Infections
WHO treatment guidelines for drug resistant tuberculosis 2016 update
Fonti
Lewinsohn, D, et. al. (2017 January 03). Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention Clinical Practice Guidelines: Diagnosis of Tuberculosis in Adults and Children. Clinical Infectious Diseases, Volume 64, Issue 2, 15 January 2017, Pages 111–115. Available online at https://academic.oup.com/cid/article/64/2/111/2811357.Accessed on 8/05/18.
Vyas, J. et. al. (2016 November 14, Updated).Sputum stain for mycobacteria.MedlinePlus Medical Encyclopedia.Available online at https://medlineplus.gov/ency/article/003724.htm.Accessed on 8/05/18.
Koirala, J. (2017 November 14, Updated). Mycobacterium Avium Complex (MAC) (Mycobacterium Avium-Intracellulare [MAI]). Medscape Infectious Diseases.Available online at https://emedicine.medscape.com/article/222664-overview.Accessed on 8/05/18.
Herchline, T. and Amorosa, J. (2017 November 9, Updated).Tuberculosis (TB).Medscape Infectious Diseases.Available online at https://emedicine.medscape.com/article/230802-overview.Accessedon 8/05/18.
Batra, V. and Ang, J. (2018 April 26, Updated).Pediatric Tuberculosis. Medscape Pediatrics:General Medicine. Available online at https://emedicine.medscape.com/article/969401-overview.Accessedon 8/05/18.
Barker,A.(2018July,Updated).Mycobacteriumtuberculosis–Tuberculosis.ARUPConsult.Available online at https://arupconsult.com/content/mycobacterium-tuberculosis.Accessed on8/05/18.

