LTOApprofondimenti
Cerca tra gli Approfondimenti
Cerca tra gli Approfondimenti
Ultima Revisione: 12.02.2019. Ultima Modifica: 01.03.2019.
Quest’articolo esamina sotto diversi punti di vista l’impatto e il ruolo che le conoscenze genetiche possono avere sulla pratica clinica.
Le applicazioni dei test genetici sono molteplici, tra le quali:
Prima di riflettere sulla possibilità di sottoporsi ad un test genetico, è utile apprendere i rudimenti di questa disciplina così da comprenderne i limiti e le potenzialità. Questo articolo fornisce tuttavia solo delle informazioni di base riguardanti la genetica umana e non può in alcun modo sostituire il colloquio con un consulente genetico.
La somma di tutte le informazioni genetiche di un individuo viene chiamata genoma. Da un punto di vista strutturale, il genoma consiste in una lunga catena di DNA (acido desossiribonucleico) avvolta a formare una doppia elica destrorsa e quindi impaccata a costituire i cromosomi. All'interno della lunga catena di DNA sono contenuti dei segmenti chiamati geni, i quali vengono utilizzati come stampo per la produzione di molecole di RNA (una sorta di "fotocopie" delle informazioni contenute nel DNA) utilizzate per trasmettere le informazioni genetiche traducendole in proteine, gli agenti principali responsabili della funzionalità dell'organismo.
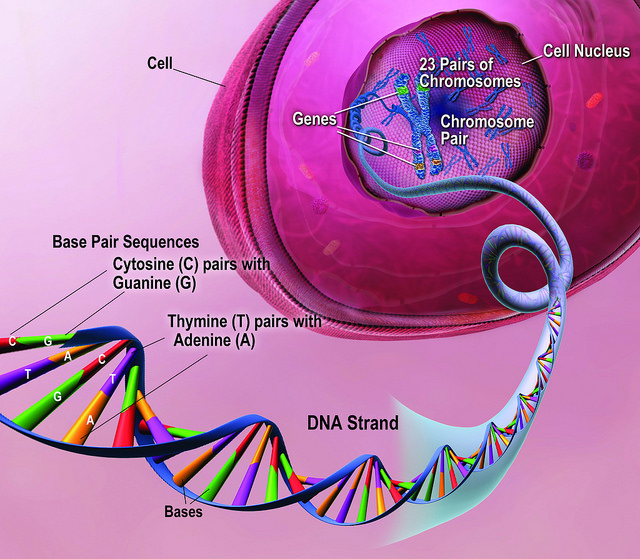
Fonte immagine: National Human Genome Research Institute
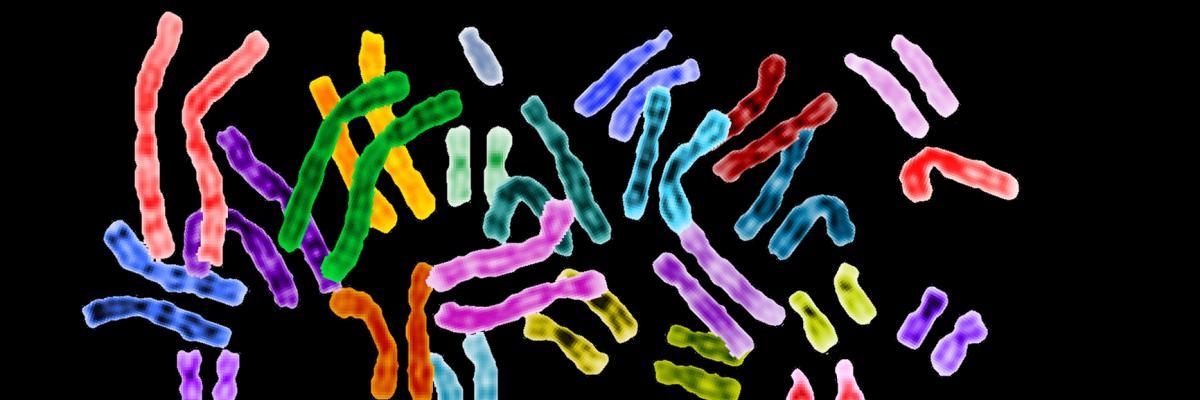
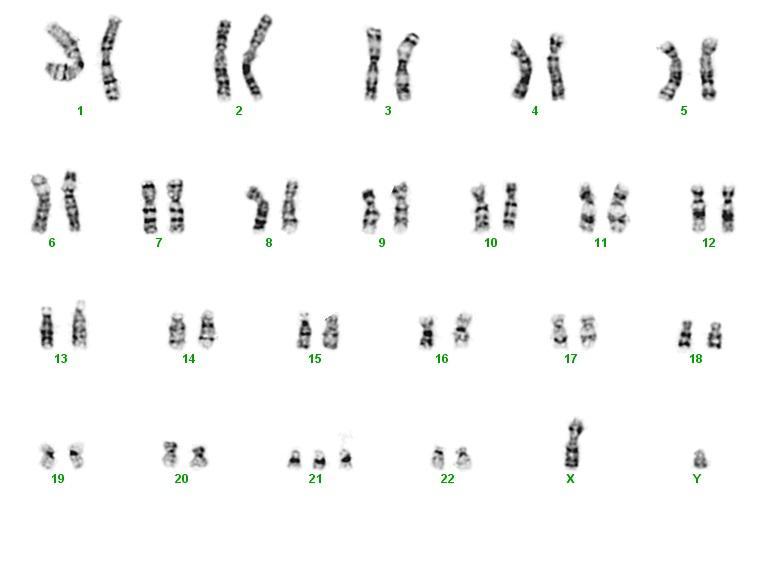
Ciascuna cellula dell'organismo contiene 23 coppie di cromosomi omologhi (in totale 46), metà di origine materna e metà di origine paterna. Delle 23 coppie di cromosomi, 22 coppie (gli autosomi) vengono identificate tramite una numerazione crescente, da 1 a 22. La restante coppia di cromosomi è composta dai noti cromosomi X e/o Y, ossia i cromosomi sessuali (o eterocromosomi). I cromosomi sessuali contengono tutte le informazioni genetiche necessarie alla determinazione del sesso, inclusi i caratteri primari e secondari; i maschi possiedono un cromosoma X ed un Y (XY) mentre le femmine due cromosomi X (XX) . I cromosomi sono contenuti nel nucleo della cellula. Esistono tuttavia piccoli frammenti di DNA contenuti in altre aree della cellula, esterne al nucleo, come quelli contenuti nei mitocondri, organelli a localizzazione citoplasmatica.

Sebbene la maggior parte delle varianti genetiche non faccia altro che aumentare la biodiversità, alcune hanno un ruolo nello sviluppo di malattie. Le variazioni genetiche che causano una malattia sono di solito chiamate "mutazioni" le quali possono essere di diversa natura e origine.
Nella tabella sottostante sono riportate alcuni esempi di mutazioni responsabili di malattie genetiche.
Alterazione Genetica | Descrizione | Esempi |
|---|---|---|
Delezione | Perdita del materiale genetico o di un pezzo di cromosoma che può interessare da una singola base azotata fino a grossi frammenti di cromosoma. | La causa più frequente di distrofia muscolare di Duchenne è la delezione di una parte del gene DMD. |
Inserzione | Aggiunta di materiale genetico (una base o un frammento di DNA) alla sequenza di DNA, spesso all'interno di un gene. | Una delle mutazioni più frequenti del gene BRCA1 (associato all'aumentato rischio di sviluppare il carcinoma alla mammella e all'ovaio) è l'inserzione di 2 nucleotidi all'interno del gene. Tale inserimento causa lo scorrimento del codice genetico e l'alterazione della proteina prodotta. |
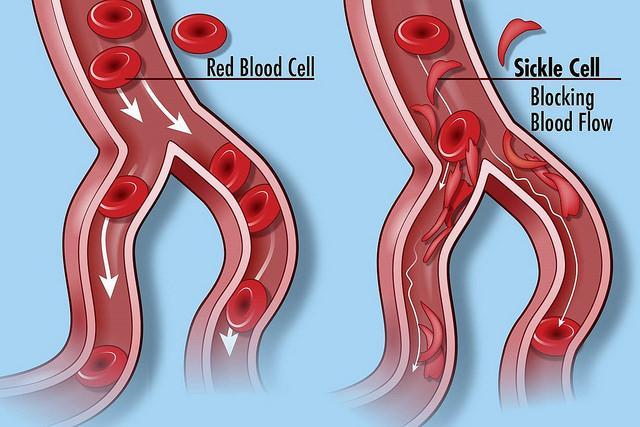
Sostituzione | Inserimento di una base o un frammento genico al posto di un altro. | Un esempio è l'anemia falciforme nella quale vi è la sostituzione di un nucleotide. Questo causa la produzione di una proteina che non è in grado di funzionare correttamente e che causa l'alterazione della forma dei globuli rossi (falcizzazione) e la conseguente anemia. |
Duplicazione | Duplicazione una o più volte di frammenti genetici presenti in alcune aree del genoma. Questo può comportare la produzione di molte più proteine rispetto al necessario che possono accumularsi o non funzionare correttamente. | La duplicazione del gene PMP22 causa una malattia dei nervi periferici chiamata malattia di Carcot-Marie-Tooth di tipo 1. |
Amplificazione | Presenza di più copie di un gene in una cellula (spesso avviene nelle cellule tumorali). | Un esempio è l'amplificazione di HER2 in alcuni tipi di cancro, in modo particolare nel cancro alla mammella. La presenza di troppe copie del gene determina la produzione eccessiva della proteina HER2 la quale è responsabile della promozione incontrollata della crescita delle cellule cancerose. |
Traslocazione cromosomica (riarrangiamento cromosomico o fusione genica) | Alcuni pezzi di cromosoma possono rompersi e riattaccarsi in altri cromosomi. Nel caso in cui vi sia un semplice scambio di frammenti di cromosomi da un cromosoma all'altro, senza l'alterazione dei geni in essi contenuti, si parla di traslocazione "bilanciata" ed è meno probabile che questa abbia conseguenze fenotipiche. Nel caso in cui parte del materiale genetico vada perso o venga duplicato durante la traslocazione, si parla invece di traslocazione "non bilanciata" che può portare con molta probabilità a patologia. | Il gene BCR-ABL1 è il frutto della traslocazione che intercorre tra un pezzo del cromosoma 9 e un pezzo del cromosoma 22. La traslocazione determina la fusione del gene ABL1, presente sul cromosoma 9, con il gene BCR, presente sul cromosoma 22. Il nuovo gene BCR-ABL1 che si crea codifica per una proteina anomala responsabile dello sviluppo della leucemia mieloide cronica(CML) e della leucemia linfoblastica acuta (ALL). |
Inversione | Un inversione è causata dalla rottura di un cromosoma in due punti con la conseguente inversione del materiale genetico presente. Come nel caso della traslocazione, l'inversione può causare perdita o duplicazione di frammenti genetici con molteplici implicazioni. | La malattia dipende dal cromosoma e i geni interessati, oltre che dalla presenza delle rotture in aree interne o esterne alle regioni codificanti (i geni) o in quelle regolatorie. |
Ripetizioni | Esistono alcune aree del DNA che normalmente presentano delle sequenze ripetute un numero definito di volte. Nel caso in cui queste ripetizioni aumentino (espansione delle sequenze ripetute), la struttura, funzione o espressione dei geni può subire un'alterazione. | Esistono molti disordini genetici causati dall'espansione delle sequenze ripetute. Alcuni esempi includono la malattia di Huntington e la sindrome dell'X fragile. |
Trisomia | Presenza di un cromosoma sovrannumerario e quindi di tre cromosomi omologhi piuttosto che due. | Alcune patologie associate alla trisomia sono la sindrome di Down (trisomia 21), la sindrome di Edwuards (trisomia 18) o la sindrome di Patau (trisomia 13). |
Monosomia | Assenza di un cromosoma e quindi presenza di un singolo cromosoma in una delle coppie omologhe. | Un esempio è la sindrome di Turner (una femmina con un solo cromosoma X invece che XX). |

È importante capire che i test genetici sono piuttosto differenti dagli altri esami di laboratorio. Essi sono infatti capaci di fornire informazioni specifiche per ciascun individuo, come formulare una diagnosi o predire la comparsa di una patologia prima della comparsa dei sintomi, fornire in termini probabilistici la possibilità di trasmettere una certa patologia alla prole e fornire informazioni riguardo le capacità di risposta ad una certa terapia. I test genetici forniscono talvolta anche informazioni riguardanti i familiari del soggetto in esame.
I test genetici di interesse clinico riguardano esami del DNA o dell’RNA che possono essere utili nella diagnosi e gestione delle patologie. Pur fornendo degli indiscussi vantaggi, esistono molti aspetti dei test genetici che devono essere considerati e valutati con l’aiuto di un consulente genetico in grado di informare correttamente i pazienti riguardo tutti i pro ed i contro relativi a ciascun test e alle conseguenze che esso può comportare. Alcuni esempi di test genetici di interesse clinico includono:
I test diagnostici genetici vengono utilizzati per la diagnosi o esclusione di patologie genetiche in individui sintomatici. Esistono centinaia di test per la diagnosi di molte patologie ereditarie. Molti di questi ricercano alterazioni in geni specifici responsabili di patologie come la fibrosi cistica, l'anemia falciforme o alcune forme particolari di distrofia muscolare.
Molte patologie ereditarie possono essere identificate indirettamente tramite la rilevazione di anomalie nei prodotti finali (proteine o metaboliti) di geni che potrebbero essere alterati. Il codice genetico contiene le informazioni per la produzione di molteplici proteine cosicché una sua variazione determina l'alterazione della produzione delle proteine corrispondenti. Un esempio è l'emofilia, una sindrome emorragica. Lo screening rileva la diminuzione di alcuni fattori della coagulazione (proteine che regolano la coagulazione) in grado di suggerire la presenza di una sindrome emorragica. I test genetici forniscono indicazioni utili per la ricerca della stessa mutazione nei familiari dell'individuo affetto.
Questo tipo di test viene perlopiù utilizzato nell’ambito della medicina forense. Il termine “test del DNA” è un termine improprio che in realtà è riferibile a qualsiasi test genetico, sia esso utilizzato per la diagnosi delle patologie, per la tipizzazione dei tessuti o per l’identificazione di persone.
Per lo scopo forense, il DNA, sia esso nucleare o mitocondriale, viene estratto a partire da molteplici campioni: sangue, capelli, tessuti, ossa ecc…. Qualsiasi materiale contenente cellule nucleate e quindi contenenti il DNA, può essere utilizzato per le analisi forensi. Il DNA mitocondriale è particolarmente utile nel caso di campioni degradati.
I test di identificazione vengono utilizzati per cercare di identificare le persone sospettate di un crimine o anche per identificare ed attribuire i resti di persone irriconoscibili a causa della decomposizione. Per questo tipo di confronti vengono analizzate le ripetizioni di sequenze di DNA chiamate microsatelliti o minisatelliti, uniche per ciascun individuo. Nella biologia forense queste metodiche vengono indicate con il termine “DNA fingerprint”, che fa riferimento ad una sorta di impronta digitale del DNA, specifica per ciascun individuo.

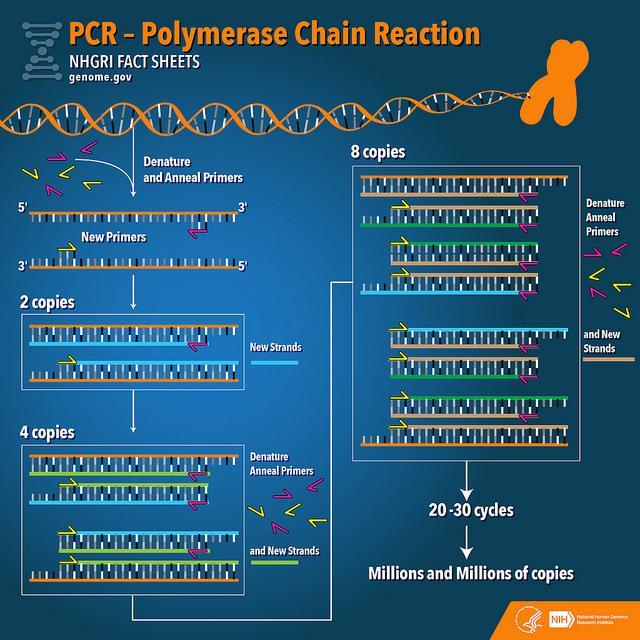
La PCR (Reazione a Catena della Polimerasi; Polymerase Chain Reaction; PCR) è una tecnica di laboratorio utilizzata molto frequentemente che consente di ottenere un numero enorme di copie di piccoli frammenti di DNA a partire da campioni contenenti quantità minime di DNA originario. Questo processo, noto come "amplificazione", consente la rilevazione e la misura dei geni d'interesse, oltre che la creazione di molteplici copie di DNA, utilizzabili per essere sequenziate o analizzate con altre tecniche. Spesso viene usata per la ricerca delle mutazioni genetiche responsabili di alcune patologie, come quelle associate con alcuni tipi di cancro o di malattie genetiche.
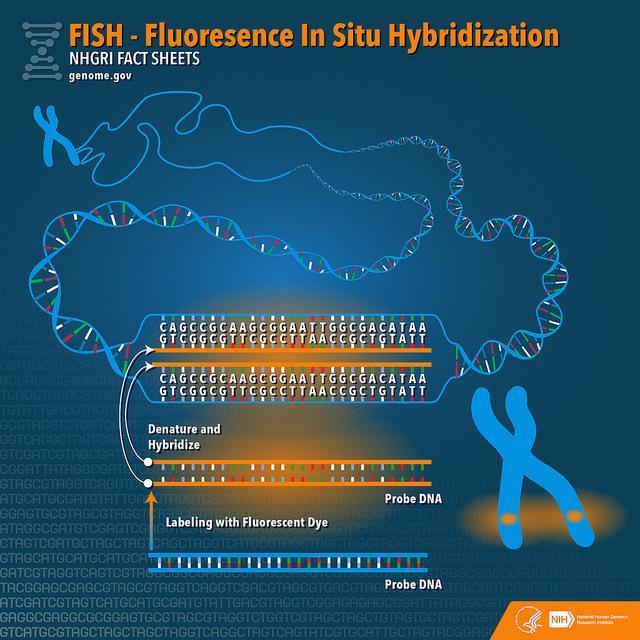
Per maggiori dettagli si rimanda alla pagina Tecniche di Laboratorio.
(Updated 2015 June 16). Deoxyribonucleic acid (DNA). National Human Genome Research Institute. Available online at https://www.genome.gov/25520880/. Accessed October 2018.
(Reviewed 2017 September 28). Studying genes. National Institutes of Health, National Institute of General Medical Sciences. Available online at https://www.nigms.nih.gov/Education/pages/Factsheet_studyinggenes.aspx. Accessed October 2018.
(Updated 2017 October 3). Genetics. Medline Plus. Available online at https://medlineplus.gov/ency/article/002048.htm. Accessed October 2018.
(2017 October 17). What is a gene? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/basics/gene. Accessed October 2018.
(2017 October 17). What is a chromosome? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/basics/chromosome. Accessed October 2018.
Tietz Textbook of Clinical Chemistry and Molecular Diagnostics. Nader Rifai. 6th edition, Elsevier Health Sciences; 2017.
(2017 October 17). What kinds of gene mutations are possible? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer#mutationsanddisorders. Accessed October 2018.
(2017 October 17). What are the different ways in which a genetic condition can be inherited? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/inheritance/inheritancepatterns. Accessed October 2018.
(2017 October 17). How do genes control the growth and division of cells? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/howgeneswork/genesanddivision. Accessed October 2018.
(2017 October 17). What are single nucleotide polymorphisms (SNPs)? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/genomicresearch/snp. Accessed October 2018.
Wang QJ, Rao SQ, Zhao YL, Liu QJ, Zong L, Han MK, Han DY, Yang WY. The large Chinese family with Y-linked hearing loss revisited: clinical investigation. Acta Otolaryngol. 2009 Jun;129(6):638-43.
November 10, 2015, National Human Genome Research Institute, Frequently Asked Questions About Genetic Disorders. Available online at https://www.genome.gov/19016930/faq-about-genetic-disorders/. Accessed November 2018
Nagan, et al. (2011 January). Laboratory guidelines for detection, interpretation, and reporting of maternal cell contamination in prenatal analysis. Journal of Molecular Diagnostics. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3069929/. Accessed October 2018.
(© 2018). What is diagnostic testing? Genes in Life. Available online at http://www.genesinlife.org/testing-services/testing-genetic-conditions/diagnostic-testing. Accessed October 2018.
Genetic testing. American Medical Association. Available online at https://www.ama-assn.org/content/genetic-testing. Accessed October 2018. Advanced genomic testing. Cancer Treatment Centers of America. Available online at http://www.cancercenter.com/treatments/cancer-genomics/. Accessed October 2018.
Van den Veyver, I. (2016 October 8). Recent advances in prenatal genetic screening and testing. F1000 Research. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5089140/. Accessed October 2018.
(2017 July 10). MammaPrint test addressed in ASCO breast cancer guideline update. American Society of Clinical Oncology. Available online at https://www.asco.org/about-asco/press-center/news-releases/mammaprint-test-addressed-asco-breast-cancer-guideline-update. Accessed October 2018.
Durmaz, A. A. et al. (2015). Evolution of genetic techniques: Past, present, and beyond. Biomed Research International. Available online at https://www.hindawi.com/journals/bmri/2015/461524/. Accessed October 2018.
(2015 April 1). BRCA1 and BRCA2: Cancer risk and genetic testing. National Cancer Institute. Available online at https://www.cancer.gov/about-cancer/causes-prevention/genetics/brca-fact-sheet. Accessed October 2018.
Ngeow, J. and Eng, C. (2016 January 13). Precision medicine in heritable cancer: when somatic tumour testing and germline mutations meet. Genomic Medicine. Available online at https://www.nature.com/articles/npjgenmed20156. Accessed October 2018.
(2017 July). Prenatal genetic screening tests. The American College of Obstetricians and Gynecologists. Available online at https://www.acog.org/Patients/FAQs/Prenatal-Genetic-Screening-Tests. Accessed October 2018.
(Reviewed 2016 February). Newborn screening tests for your baby. March of Dimes. Available online https://www.marchofdimes.org/baby/newborn-screening-tests-for-your-baby.aspx. Accessed October 2018.
What is a DNA fingerprint? Wellcome Genome Campus. Available online at https://www.yourgenome.org/facts/what-is-a-dna-fingerprint. Accessed October 2018. (2017 November 21). What are the types of genetic tests? Genetics Home Reference. Available online at https://ghr.nlm.nih.gov/primer/testing/uses. Accessed November 2018.
Rehm, H.L. (2013 April). Disease-targeted sequencing: a cornerstone in the clinic. Nature Reviews Genetics. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3786217/. Accessed October 2018.
Katsanis, S. H. and Katsanis N. (2013 June). Molecular genetic testing and the future of clinical genomics. National Review of Genetics. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4461364/. Accessed October 2017. Behjati, S. and Tarpey P.S. (2013 December). What is next generation sequencing? Archives of Disease in Childhood. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3841808/. Accessed October 2018.
Shen T., et al. (2015 June 17). Clinical applications of next generation sequencing in cancer: from panels, to exomes, to genomes. Frontiers in Genetics. Available online at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4469892/. Accessed October 2018.
Moynihan, T. (2015 June 30). Gene expression profiling for breast cancer: What is it? Mayo Clinic. Available online at https://www.mayoclinic.org/diseases-conditions/breast-cancer/expert-answers/gene-expression-profiling/faq-20058144. Accessed October 2018
(2015 August 27). DNA microarray technology. National Human Genome Research Institute. Available online at https://www.genome.gov/10000533/dna-microarray-technology/. Accessed October 2018.
(Updated 2015 December 18). DNA sequencing. National Human Genome Research Institute. Available online at https://www.genome.gov/10001177/dna-sequencing-fact-sheet/. Accessed October 2018.
Benowitz, S. (2016 March 29). New study challenges gold standard for validating DNA sequencing results. National Human Genome Research Institute. Available online at https://www.genome.gov/27564480/2016-news-feature-new-study-challenges-gold-standard-for-validating-dna-sequencing-results/. Accessed October 2018.
Hamilton, A. et al. (2016 May 10). Concordance between whole-exome sequencing and clinical Sanger sequencing: implications for patient care. Molecular Genetics and Genomic Medicine. Available online at http://onlinelibrary.wiley.com/doi/10.1002/mgg3.223/full. Accessed October 2018.
Sabour L., et al. (2017 April). Clinical applications of next-generation sequencing in cancer diagnosis. Pathology and Oncology Research. Available online at https://link.springer.com/article/10.1007/s12253-016-0124-z. Accessed October 2018.
(© 2017). What is diagnostic testing? Genes in Life. Available online at http://www.genesinlife.org/testing-services/testing-genetic-conditions/diagnostic-testing. Accessed October 2018.
(© 2017). What is genotyping and expression profiling? Genotyping and Coriell Institute for Medical Research. Available online at https://www.coriell.org/research-services/genotyping-microarray/what-is-genotyping-and-expression-profiling. Accessed October 2018.
(August 27, 2015) National Human Genome Research Institute, DNA Microarray. Available online https://www.genome.gov/10000533/dna-microarray-technology/ Accessed October 2018.