LTONews
Cerca tra le News
Cerca tra le News
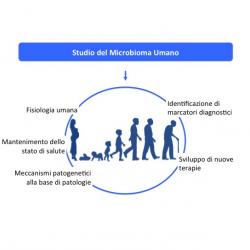
Il microbiota umano è l’insieme di tutti i microrganismi che colonizzano la superficie ed i vari distretti del corpo umano, mentre il corredo genetico di tutti questi microrganismi è definito microbioma. Negli ultimi anni, lo studio del microbioma umano ha avuto un enorme sviluppo, grazie alla disponibilità di nuove tecnologie in grado di analizzare con un’elevata risoluzione intere comunità microbiche. Queste ricerche scientifiche non solo hanno permesso di identificare microrganismi in un numero crescente di organi e tessuti, ma hanno anche reso evidente il loro contributo in numerose funzioni necessarie per la conservazione dello stato di salute dell’ospite/uomo. E’ oggi noto, che il solo microbiota intestinale umano sia costituito da oltre 1000 specie diverse che codificano per circa 5 milioni di geni coinvolti in funzioni importanti per il mantenimento di un corretto equilibrio di varie funzioni dell’organismo, lo sviluppo fisiologico ed il mantenimento dello stato di salute umana (quali digestione di sostanze contenute negli alimenti, sintesi di vitamine ed amminoacidi essenziali, detossificazione di composti tossici, protezione nei confronti di agenti patogeni).
Oggi sappiamo che la relazione dell’uomo con il suo microbioma ha origine già in epoca perinatale. Si è ritenuto per anni, che nel sacco amniotico il feto fosse in condizioni di sterilità; recenti evidenze hanno messo in discussione questo dogma centrale della medicina della riproduzione: batteri sono stati identificati nel meconio, nel liquido amniotico, nella placenta e nel sangue cordonale, suggerendo l’esistenza di un microbioma prenatale. Successivamente, durante il passaggio nel canale del parto, il nascituro viene esposto ad una serie di microrganismi e viene quindi rapidamente colonizzato: questo processo è fondamentale per il corretto sviluppo del sistema immunitario. Infine, durante l’età adulta, anche se influenzato da una varietà di stimoli inclusi il tipo di dieta, l'attività fisica, i viaggi, eventuali malattie, cicli ormonali e terapie, il microbioma diventa abbastanza stabile e, nonostante le numerose differenze tra individui diversi, appare caratterizzato da un nucleo comune che si ritiene sia coinvolto in funzioni importanti per la fisiologia umana.
L’aumento delle conoscenze relative al microbioma umano ed alle sue funzioni ha rinforzato progressivamente l’idea che l'equilibrio tra ospite, microbioma ed ambiente giochi un ruolo fondamentale nel mantenimento dello stato di salute. Ad oggi, alterazioni quantitative e/o qualitative nella composizione del microbioma sono state dimostrate in un numero crescente di patologie. E’ noto che specifiche alterazioni microbiche sono presenti in numerose patologie, non solo intestinali (ad esempio, obesità, celiachia, morbo di Crohn e rettocolite ulcerosa), ma anche in malattie tipicamente extra-intestinali: nell’autismo, ad esempio, è stata dimostrata la presenza di alterazioni del microbioma intestinale che, modificando la permeabilità dell’intestino, determinano alterazioni comportamentali tipiche dello spettro autistico. Pertanto, lo studio del microbioma umano apre nuove importanti prospettive per comprendere i meccanismi sottesi allo sviluppo di specifiche patologie. Inoltre, l’identificazione di specifiche alterazioni, non solo potrebbe fornire un nuovo strumento diagnostico e prognostico con l’introduzione del microbioma quale nuovo biomarcatore, ma potrebbe anche aprire la strada allo sviluppo di nuovi approcci terapeutici.
Con l'aumento delle conoscenze relative a funzioni del microbioma intestinale ed al suo ruolo nel mantenimento del corretto equilibrio delle funzioni fisiologiche, sta diventando sempre più possibile sviluppare nuove strategie terapeutiche basate sulla manipolazione del microbioma. Infatti, a differenza del genoma umano, il microbioma umano può essere facilmente modificato attraverso la somministrazione di antibiotici, probiotici e prebiotici. Inoltre, la nutrizione enterale e il trapianto di microbioma hanno anche dimostrato la loro efficacia in alcune condizioni specifiche, come ad esempio nel trattamento delle malattie infiammatorie croniche intestinali (morbo di Crohn e rettocolite ulcerosa) e dell’infezione da Clostridium difficile.
Questi studi, seppure ancor preliminari, mostrano come aumentando le conoscenze relative al microbioma umano ed al suo ruolo nella patogenesi delle malattie, la possibilità di trattare (o almeno di attenuare) condizioni specifiche mediante la manipolazione del microbioma diventi sempre più attuale. Tuttavia, è importante sottolineare che è necessario condurre accurati studi preclinici e clinici per valutare l’efficacia e la sicurezza di questo tipo di interventi prima che possano realmente entrare nella pratica clinica di routine.
Come discusso nelle precedenti sezioni, diversi studi clinici suggeriscono che lo studio della composizione quali/quantitativa del microbioma umano, nei vari distretti dell’organismo, possa diventare un utile strumento nell’iter diagnostico di numerose patologie. In quest’ottica appare fondamentale disporre di metodologie analitiche che permettano l’analisi accurata e rapida del microbioma. Attualmente, l’analisi della sequenza dell’RNA ribosomale batterico 16S mediante tecniche di sequenziamento ad elevata produttività (Next Generation Sequencing) rappresenta la tecnica di elezione per la caratterizzazione completa del microbioma umano. L’associazione con tecniche microbiologiche più tradizionali, e anche con quelle di tipo biochimico-analitico-strumentale, come la spettrometria di massa, per l’identificazione delle specie batteriche in una popolazione o in un particolare ambiente tissutale o liquido biologico, può rappresentare un ulteriore vantaggio grazie alla possibilità di isolare e caratterizzare, dal punto di vista molecolare e funzionale, specifici ceppi batterici isolati nei campioni in esame. Visti i rapidi progressi tecnologici è facile ipotizzare che l’analisi del microbioma possa entrare presto nell’attività clinica di routine e che il laboratorio di Biochimica Clinica e Biologia Molecolare Clinica possa fornire un valido contributo in tal senso sia in fase di definizione diagnostica sia durante il monitoraggio per valutare l’efficacia di specifiche terapie.
Valeria D’Argenio - CEINGE-Biotecnologie Avanzate, Napoli
D'Argenio V. Human Microbiome Acquisition and Bioinformatic Challenges in Metagenomic Studies. Int J Mol Sci. 2018 Jan 27;19(2). pii: E383. doi: 10.3390/ijms19020383